Nel XVI e XVII secolo si può parlare di una «preistoria» della chimica ancora molto legata all’alchimia. L’articolo mostra i primi tentativi di formulare ipotesi sulle reazioni chimiche, spesso ancora legati a residui di aristotelismo, ma in alcuni casi già indirizzati a cercare le leggi di interazione nel mondo microscopico: proprio in questa direzione il contributo di Newton (recentemente riscoperto), pur non avendo portato a una formulazione teorica precisa è stato prezioso come stimolo per i ricercatori del secolo successivo, fino all’inizio vero e proprio della chimica con gli esperimenti di Lavoisier.
Nel testo dal titolo Personaggi e scoperte della fisica (1) si legge «[…] il genio di Newton non si estendeva alla chimica: il fondatore della fisica-matematica non è infatti importante per la storia della chimica. Forse era necessaria una diversa forma mentale per fare progressi in questa scienza». 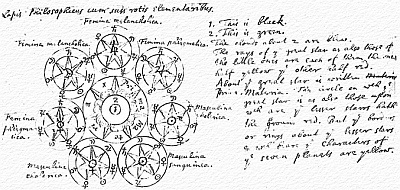 [A sinistra: Appunti di Newton sull’alchimia (Lapis Philosophicus, manoscritto n. 416). fisa.altervista.org]
[A sinistra: Appunti di Newton sull’alchimia (Lapis Philosophicus, manoscritto n. 416). fisa.altervista.org]
Oggigiorno (rispetto al 1983) abbiamo avuto la fortuna che è stata studiata la grande collezione di libri di alchimia e relativi manoscritti originali di Isaac Newton. Tutto ciò ha contributo alla preparazione del suo posto nella storia della chimica. È stato constatato essere un acuto, originale e accurato ricercatore con una larga influenza nel XVII e XVIII secolo. Nel catalogo della sua personale libreria (2) sono citati almeno un centinaio di libri di chimica e alchimia e sono registrati e catalogati molti manoscritti.
Due sono gli argomenti concettuali base che saranno trattati in questo articolo. Il primo riguarda un importante lavoro di ricerca per fondare una «dottrina» della chimica, o meglio, della «protochimica» del XVIII secolo. Il secondo concerne la sorgente di descrizione di reazioni chimiche, con relativi dettagli sperimentali, contenuti nell’appendice Questioni di studio al trattato Ottica (3), una vera miniera per un chimico pratico del XVII secolo. Queste Questioni di studio contengono anche proposte di ricerche e di riflessioni nel campo generale delle scienze della natura.
Il passaggio graduale dall’alchimia alla chimica nei secoli XVII e XVIII
Ogni studioso di questo periodo storico, con inclinazione alle materie scientifiche, incontrò inevitabilmente le applicazioni teoriche e pratiche dell’alchimia. Quest’ultima, che aprì la strada alla chimica, fu una disciplina completa avente lo scopo di portare il «macrocosmo» (l’Universo) in stretta relazione con il «microcosmo» (inteso come l’essere umano). Peraltro una buona parte dell’alchimia, ereditata nel Rinascimento dall’antichità classica, fu «scientifica» e di natura altamente tecnica.
Quali erano i fini principali dell’alchimia? La trasmutazione dei metalli più vili in argento e oro; la creazione di un elisir della giovinezza e nello stesso tempo il perfezionamento e la purificazione dell’anima dell’alchimista stesso. È facilmente immaginabile come, sotto il velo dell’ascesi e dell’esoterismo, persone disoneste lucrarono, con l’inganno, guadagni in potere e ricchezze.  È superfluo notare quale fosse stata l’opinione di Newton a riguardo della degenerazione dell’alchimia; comunque si riportano qui alcuni passi di una lettera scritta a Henry Oldenburg (1676), segretario della Royal Society di Londra: «Ieri leggendo gli ultimi due numeri delle Philosophical transactions ho avuto l’occasione di esaminare l’insolito esperimento di Boyle sulla forma di riscaldamento dell’oro e del mercurio […]. Pertanto non dubito che la grande saggezza del nobile autore lo spingerà a un profondo silenzio, fino a quando egli non avrà compreso le possibili conseguenze dei fatti per esperienza propria […] perché ben altre cose esistono oltre alla transmutazione dei metalli (se quei grandi simulatori non hanno propagato fanfaronate) che debbon essere validamente approfondite […] vi prego di mantenere questa lettera mia, privata. Il vostro umilissimo servo Isaac Newton».
È superfluo notare quale fosse stata l’opinione di Newton a riguardo della degenerazione dell’alchimia; comunque si riportano qui alcuni passi di una lettera scritta a Henry Oldenburg (1676), segretario della Royal Society di Londra: «Ieri leggendo gli ultimi due numeri delle Philosophical transactions ho avuto l’occasione di esaminare l’insolito esperimento di Boyle sulla forma di riscaldamento dell’oro e del mercurio […]. Pertanto non dubito che la grande saggezza del nobile autore lo spingerà a un profondo silenzio, fino a quando egli non avrà compreso le possibili conseguenze dei fatti per esperienza propria […] perché ben altre cose esistono oltre alla transmutazione dei metalli (se quei grandi simulatori non hanno propagato fanfaronate) che debbon essere validamente approfondite […] vi prego di mantenere questa lettera mia, privata. Il vostro umilissimo servo Isaac Newton».  Vi sono due aspetti dell’alchimia da tenere in considerazione. Da una parte essa era una scienza applicata e i suoi obiettivi erano pratici e legati al commercio; dall’altra si configurava come una specie di esoterismo e uno stile di vita un po’ ascetico. A noi interesserà principalmente il primo aspetto in vista di considerarlo come una vera e propria «fase embrionale della chimica» ovvero, se si vuole più semplicemente, una «protochimica».
Vi sono due aspetti dell’alchimia da tenere in considerazione. Da una parte essa era una scienza applicata e i suoi obiettivi erano pratici e legati al commercio; dall’altra si configurava come una specie di esoterismo e uno stile di vita un po’ ascetico. A noi interesserà principalmente il primo aspetto in vista di considerarlo come una vera e propria «fase embrionale della chimica» ovvero, se si vuole più semplicemente, una «protochimica».
Proseguendo sempre nello studio del primo aspetto, l’obiettivo ultimo degli alchimisti sembra essere stato quello di imitare e accelerare quei processi, che in natura avvengono più lentamente e in un modo meno perfetto, per riuscire a ottenere gli stessi risultati più rapidamente e a costi ridotti. Cercarono in definitiva di usare le risorse naturali nel modo più razionale possibile.
Processi chimici quali ossidazione, riduzione, soluzione, fusione e lega erano ben noti agli alchimisti. Zolfo e mercurio mostravano gli effetti più spettacolari, per quel che riguardava trasformazione di colore e di materia; il termine alcool è arabo, ma originariamente indicava la fine polvere metallica (di solito antimonio ridotto in polvere), che le donne del vicino oriente mettevano sulle palpebre.
Anche la strumentazione degli alchimisti divenne d’uso corrente in questa fase di «protochimica». L’«alambicco», semplice strumento di distillazione, era formato da un vaso di forma pressoché sferica e da un coperchio di forma conica allungata che trasportava il prodotto distillato in un contenitore atto a riceverlo. Poi vi era il «forno» cioè una piccola torre a cupola contenente un recipiente di forma ovale, posto in un bagno di sabbia sopra il fuoco; con questo insieme era possibile mantenere una temperatura costante.
Newton si era allestito così un laboratorio proto-chimico nel quale si poteva sbizzarrire in ricerche sulle reazioni chimiche più singolari e sino allora non preparate né studiate. I risultati sono raccolti in prevalenza nella serie di trentuno Questioni di studio, ovvero proposte di ricerca, designate d’ora in poi con la lettera Q seguita dal relativo numero «i» con «i» = 1, 2, 3 … 31.
Molti sono i concetti e le meditazioni di Newton conseguenti a questo lavoro scientifico nel suo laboratorio, ci limitiamo qui a ricordare quello relativo alla Q30 utile a rendere evidente il «ruolo chimico attivo dell’aria».
Sino al XVII secolo era dominante il pensiero dei peripatetici (di osservanza aristotelica) per il quale i quattro elementi fondamentali della natura (aria, acqua, terra, fuoco) avevano soltanto funzioni fisiche, ma non chimiche.  Ossia, per esempio, l’aria, secondo queste vedute, non si combinava con le altre sostanze con cui entrava in contatto. I peripatetici e altri pensatori astratti erano inclini a credere che le particelle d’aria potessero solo inserirsi come corpi estranei nei «minuscoli pori» delle sostanze solide.
Ossia, per esempio, l’aria, secondo queste vedute, non si combinava con le altre sostanze con cui entrava in contatto. I peripatetici e altri pensatori astratti erano inclini a credere che le particelle d’aria potessero solo inserirsi come corpi estranei nei «minuscoli pori» delle sostanze solide.
[A destra: Stephen Hales (1677-1761) in un ritratto di Thomas Hudson (1759)]
Conseguentemente l’aria atmosferica veniva considerata come un medium inerte costituito da particelle elastiche nel quale si trovano dispersi i corpuscoli di varie sostanze. Newton falsificò questa elucubrazione nell’ambito nuovo del metodo galileiano sperimentale, dell’ormai nascente scienza moderna.
A commento di questa analisi sperimentale, Newton afferma nella Q30: «I corpi densi, per effetto della fermentazione si rarefanno in diversi generi di aria; e quest’aria, per effetto della fermentazione, ma qualche volta senza di essa, ritorna entro i corpi densi».
Questi esperimenti vengono ripresi da Stephen Hales (4) in un suo trattato (1727), nel quale, dopo aver descritto un dispositivo che dimostra direttamente il ruolo chimico dell’aria (si veda riquadro), si esprime così: «L’illustre Sir I. Newton osserva nella Q30 questi fatti, della cui verità abbiamo dato qui prova evidente mediante molti esperimenti eseguiti».
Ovviamente questo ruolo chimico dell’aria sarà riconfermato assai più tardi dallo stesso Lavoisier.
L’esperimento di Hales conferma gli esperimenti di Newton
L’apparato piedestallo impiegato da Stephen Hales è rappresentato nell’immagine che segue. |
Le dottrine della chimica nel XVII secolo. Emergenza del modello newtoniano
Per il secondo argomento occorre soffermarci per esaminare quali fossero le dottrine per la chimica, o meglio «protochimica» del XVII secolo. Il termine dottrina qui sta a indicare la teoria generale dei processi chimici: essa è composta da ipotesi di base, elaborazione e interpretazione dei fatti, enunciazione di leggi, elencazione di regole e quant’altro. È opportuno ricordare che in Europa non esisteva, a quel tempo, «una sola tradizione teorica chimica», bensì esistevano diversi tipi di approccio al mondo dell’esperienza.  In breve sintesi vi erano tre differenti modi di approccio al mondo chimico: la spiegazione corpuscolare dei cartesiani, la spiegazione newtoniana in termini di attrazione intercorpuscolare e infine la spiegazione basata sui «principi».
In breve sintesi vi erano tre differenti modi di approccio al mondo chimico: la spiegazione corpuscolare dei cartesiani, la spiegazione newtoniana in termini di attrazione intercorpuscolare e infine la spiegazione basata sui «principi».
[A destra: Nicolas Lemery (1645-1715)]
Conviene parlare della prima e della terza, per poi analizzare quella vincente newtoniana, nelle sue applicazioni alle reazioni chimiche. La prima è ben descritta in un’opera di Nicolas Lemery dal titolo Cours de Chymie.
Questo testo rappresenta la «summa» del meccanicismo cartesiano nell’ambito della chimica teorica.  Le reazioni chimiche erano considerate come il risultato di combinazioni e separazioni di entità permanenti ossia di particelle o corpuscoli. Il compito del filosofo naturale era quello di spiegare queste trasformazioni.
Le reazioni chimiche erano considerate come il risultato di combinazioni e separazioni di entità permanenti ossia di particelle o corpuscoli. Il compito del filosofo naturale era quello di spiegare queste trasformazioni.
In questo tentativo di spiegazione scientifica venivano attribuite ai corpuscoli delle determinazioni particolari: il movimento e le forme specifiche diverse. L’attenzione dello scienziato francese si concentrò esclusivamente sulle forme immaginarie, delle particelle, ipotizzate per spiegare le proprietà delle sostanze. Il principio della ricerca di Lemery si può formulare così: «Le particelle della materia non sono percepibili dai sensi, cioè non si può individuare né la loro grandezza, né la loro forma: non si può far altro che supporle sulla base di effetti esterni».
Sennonché la teoria di Lemery era finita in un vicolo cieco: ogni fenomeno era suscettibile di interpretazione mediante l’artificio di una forma specifica particolare.
Il terzo tipo di spiegazione è incentrato sull’opera del tedesco Georg Ernst Stahl e può essere visto come una reazione alle teorie di tipo cartesiano.  Stahl rigettò le punte e le sfere (cioè la forma) di Lemery, poiché, come testé detto, ogni fenomeno richiedeva un tipo caratteristico di particella (annullando così lo statuto proprio di ogni corretta teoria). Inoltre queste particelle potevano solo essere «postulate» e non apparivano in alcun modo suscettibili di dimostrazione sperimentale.
Stahl rigettò le punte e le sfere (cioè la forma) di Lemery, poiché, come testé detto, ogni fenomeno richiedeva un tipo caratteristico di particella (annullando così lo statuto proprio di ogni corretta teoria). Inoltre queste particelle potevano solo essere «postulate» e non apparivano in alcun modo suscettibili di dimostrazione sperimentale.
[A destra: Georg Ernst Stahl (1659-1734)]
Dunque la chimica doveva essere costruita a partire dai principi, cioè da ipotetiche sostanza semplici fondamentali. In polemica contro i modelli dei meccanicistici, Stahl oppose, alle particelle, i principi che conferivano qualità e che esibivano in misura eccezionale queste qualità. Egli aveva rifiutato i quattro elementi dei peripatetici (aria, acqua, terra e fuoco) come principi delle sostanze miste, privilegiando però l’acqua e un particolare tipo di terra. Ma queste ultime non agivano solo come componenti materiali dei corpi misti. Esse agivano anche come «strumenti»; cioè operavano sia come agenti fisici sia come agenti chimici, a differenza dell’aria e del fuoco che avevano il solo ruolo di agenti fisici necessari allo sviluppo dell’azione chimica.
Introducendo la distinzione elementi e strumenti, Stahl tentò di conciliare le diverse tradizioni chimiche, che erano in forte contrasto tra loro, delle quali egli si sentiva continuatore. Le vedute di Stahl, peraltro, erano state, almeno in parte, confutate dagli esperimenti di Stephen Hales che abbiamo sopra citati, particolarmente per il carattere semplicemente strumentale che Stahl aveva attributo all’aria.
Il punto di vista di Newton
Ritorniamo ora a Newton e assumiamo innanzitutto che egli aveva esteso il concetto di attrazione universale al mondo degli atomi attribuendo a quest’ultimi tale proprietà. Newton non introduce mai la nozione di etere, ma parla sempre di forza tra particelle: attribuisce forze direttamente alle particelle materiali senza l’interposizione di un medium etereo (5).
Secondo Newton le particelle si muovono sotto l’influenza di una forza che egli denotò con il semplice termine di «attrazione». Ma, a differenza della attrazione gravitazionale, che crea una forza universale variante solo in base alla massa e alla distanza, l’attrazione chimica era selettiva e variava in ogni coppia di composti chimici. Questa specie di attrazione aveva un raggio di attrazione assai complesso: l’addizione di un composto chimico a un altro composto poteva alterare l’attrazione di quest’ultimo rispetto a un terzo e così via. Le «particelle dure», come le definisce l’atomista Newton, ossia gli atomi che costituiscono i corpi, sono dotati di virtù o forze mediante le quali agiscono a distanza l’uno sull’altro, per produrre le reazioni chimiche. Nelle Questioni di studio (Q), citate in precedenza, si ritrova una vera e propria «miniera» di rapporti descrittivi di reazioni chimiche, commentate spesso da un’analisi, per così dire, micro-dinamica del moto delle particelle interagenti (6).
 In sostanza Newton indicò agli scienziati futuri il compito di indagare le proprietà di questa attrazione chimica, poiché da essa dipendevano le principali operazioni chimiche.
In sostanza Newton indicò agli scienziati futuri il compito di indagare le proprietà di questa attrazione chimica, poiché da essa dipendevano le principali operazioni chimiche.
[A sinistra: L’ultimo ritratto di Isaac Newton (1642-1727), dipinto da E. Seaman]
La materia è costituita da atomi e sono i movimenti attrattivi e repulsivi di questi atomi che determinano la natura dei corpi. Come hanno dimostrato Arnold Thackray (7) e Robert Schofield (8), Newton fornì al secolo XVIII un programma di indagine per la costruzione di una teoria della materia fondata sul concetto di forza particellari.
I sostenitori della teoria newtoniana, nella prima metà del Settecento, non sono soltanto presenti in Inghilterra, ma anche in Olanda (Willem J. s’Gravesande e Pieter van Musschenbroek) e in Francia (Georges L. Leclerc conte di Buffon e Pierre L. Moreau de Maupertuis). Si trattò in effetti di un grande movimento di ricerca di un costrutto teorico di leggi, al fine di una quantificazione della chimica delle affinità.
Si riporta qui, in chiusura di paragrafo, un passo della Q31, particolarmente interessante per la perspicuità del ragionamento e per l’intuizione dei fenomeni microscopici sottostanti assai profonda: «Infatti, prima di indagare intorno alla causa efficiente dell’attrazione, dobbiamo apprendere dai fenomeni della natura quali corpi si attraggono a vicenda e quali sono le leggi e le proprietà dell’attrazione. Le attrazioni di gravità, del magnetismo e dell’elettricità, si estendono a distanze molto grandi e pertanto sono state osservate mediante comuni occhi, ma ce ne possono essere altre che si estendono a distanze talmente piccole da essere sfuggite, fino ad ora, all’osservazione; e forse l’attrazione elettrica può estendersi a tali piccole distanze, anche senza essere eccitate per frizione».
Lo studio sperimentale delle reazioni chimiche
Ineguagliabile è la vivacità con la quale sono descritte le seguenti reazioni, da Newton, sempre nella Q31: «E allorché l’acqua e l’olio di vetriolo versati successivamente nel medesimo vaso diventano, mescolandosi, molto caldi, questo calore non lascia supporre un grande movimento nelle parti dei liquidi? E questo movimento non lascia supporre che le parti dei due liquidi, nel mescolarsi, si combinino con violenza, e che per conseguenza si precipitino l’uno verso l’altro con moto accelerato? E quando l’acqua forte o lo spirito di vetriolo versato sopra la limatura di ferro, dissolve la limatura con grande calore ed ebollizione, questo caldo e questa ebollizione non sono causati da un movimento violento delle parti, e questo movimento non lascia supporre che le parti acide del liquido si precipitino verso le parti del metallo con violenza, ed entrino impetuosamente nei suoi pori finché giungono tra le particelle più esterne e la massa principale, e, circondando queste particelle, le separano dalla massa principale e le mettono in condizione di galleggiare separatamente nell’acqua? E il fatto che particelle acide, che separatamente, distillerebbero con un moderato calore, non si separeranno dalle particelle di metallo se non con un calore molto violento, non conferma una mutua attrazione tra loro?».
In questo passo, dallo stile quasi icastico, in cui si descrivono alcune reazioni chimiche, balzano alla mente le sensate osservazioni, in perfetta stesura galileiana, in forma di interrogativi retorici del tipo: «se osservando i fatti … non succederà questo o quest’altro?» presupponendo la risposta del lettore: ma certo che è così!
In realtà questa «protochimica» secentesca di Newton era certamente carente di una sua grammatica e sintassi precisa come anche una corretta nomenclatura delle varie sostanze in gioco, diversa da quella approssimativa, propria del XVII secolo. Newton non costruì alcun sistema chimico confrontabile al suo sistema dell’Universo, se non piuttosto un sistema mettendo insieme una teoria particellare della materia con una profonda conoscenza sperimentale della «protochimica».
D’altra parte Antoine L. Lavoisier (1743-1794), iniziando da par suo la chimica moderna, non poteva non constatare che le reazioni chimiche rispettavano la costanza della massa totale della materia, sia prima che dopo l’avvenuta reazione. Ma questa è la legge della costanza della massa di Newton. Quanto precede dimostra che Newton è un chimico anche se non vi è una scoperta positiva di chimica associata al suo nome; ma con la sua investigazione egli aiutò a far progredire la chimica sino al suo ingresso come una vera scienza della natura nel XVIII e IX secolo.
Alcune considerazioni conclusive
Abbiamo esaminato l’opera teorica e pratica di Newton, in ordine alla nascente scienza chimica, e ne abbiamo constato l’importanza nonostante le imprecisioni e la scarsa proprietà di linguaggio, caratteristiche di ogni scienziato di quel campo, nella seconda metà del Seicento.  Resta comunque da dedicare un cenno all’alchimia intesa come disciplina di sapienza tradizionale quale fu coltivata da Newton.
Resta comunque da dedicare un cenno all’alchimia intesa come disciplina di sapienza tradizionale quale fu coltivata da Newton.
La traccia che resta nelle opere a stampa della sua attività alchemica può sembrare modesta, ma una più approfondita conoscenza scaturisce riflettendo sui resoconti dei suoi esperimenti quali quelli riportati nelle Questioni, nei Principia e in altri articoli separati.
Secondo studiosi della storia della scienza contemporanei, è molto probabile che l’interesse di Newton(9) per l’attività manuale agli apparecchi alchemici e l’attività di sorveglianza delle reazioni, fosse connesso con la dimensione spirituale dell’alchimia, intendo dire come il perfezionamento dell’anima dell’alchimista inteso in quanto fine.  Sappiamo dalla testimonianza di un suo assistente che, nel periodo in cui il Nostro stava scrivendo i Principia, si occupava anche assiduamente di alchimia, seguendo il comportamento del forno durante i suoi esperimenti proto-chimici.
Sappiamo dalla testimonianza di un suo assistente che, nel periodo in cui il Nostro stava scrivendo i Principia, si occupava anche assiduamente di alchimia, seguendo il comportamento del forno durante i suoi esperimenti proto-chimici.
Ecco le parole dell’assistente: «Per sei settimane in primavera e sei in autunno, il fuoco non era quasi mai spento in laboratorio, che era ben fornito di materiali per chimica come recipienti, gli alambicchi, i crogiuoli eccetera […]».
Armando Massarenti (10), studioso contemporaneo di Newton, così si esprime al riguardo: «Se Newton può essere considerato anche un maestro del metodo sperimentale, non v’è dubbio che la sua maestria si formò anche tra gli alambicchi e i fornetti. È molto probabile, anzi, che l’interesse di Newton per l’attività manuale, spesso richiesta dalla sperimentazione come dall’alchimia, fosse la principale fonte di gratificazione della sua vita».
Vittorio Banfi
(già membro del Centro di Astrodinamica “G. Colombo” di Milano)
Note bibliografiche e varie
- E. Segrè, Personaggi e scoperte della Fisica, vol. I, Arnoldo Mondadori, Milano 1983.
- J. Harrison, The Library of Isaac Newton, Cambridge University Press, 1978.
- I. Newton, Opticks, Dover Publications, Inc., New York 1952.
- S. Hales, Vegetable Staticks, Scientific Book Guild, Beaverbooks, Newspapers, Limited, London 1961.
- M. Boas, Newton chemical papers, Osiris, Vol.10, section IX, Papers and letters, 1958.
- Per approfondire lo status delle dottrine chimiche nel XVII secolo vedere, nel testo Filosofia, scienza, politica nel Settecento francese, a cura di P. Rossi, Ed. CLUFS, Firenze 1978, il capitolo di F. Abbri Gli elementi e la natura del fuoco nella chimica francese: 1750-1770.
- A.Thackray, Atoms and Powers: an essay of newtonian matter-theory and the development of Chemistry, Cambridge Mass., 1970.
- [8] R. Schofield, Mechanism and materialism, British Natural Philosophy in the Age of Reason, Princeton 1970.
- M. White, Newton, l’ultimo mago, Rizzoli, Milano 2001.
- A. Massarenti, Newton vita, pensiero, opere scelte, Il Sole 24 ORE Cultura, 2006.
© Pubblicato sul n° 46 di Emmeciquadro

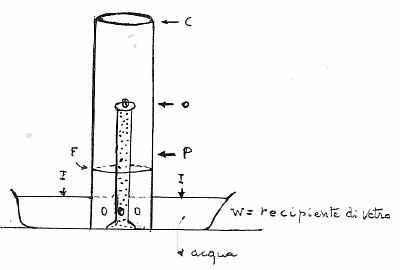 W è un recipiente contenente acqua, appoggiato su un banco; P è una colonna di sopporto solidale con W.
W è un recipiente contenente acqua, appoggiato su un banco; P è una colonna di sopporto solidale con W.