Una rubrica per guidare i bambini della scuola primaria ad «accorgersi» della varietà dei fenomeni fisici presenti nella realtà quotidiana. Per dare soddisfazione a quella curiosità infantile, definita «sacra» da Albert Einstein e tipica dei grandi scienziati, ma che è spesso mortificata da approcci ludici o fantasiosi se non addirittura aridamente formalistici.«Zio Albert» invita i suoi piccoli lettori a riflettere sull’esperienza familiare del caldo e del freddo, per comprendere il significato dei termini scientifici calore e temperatura, usati anche nel lessico comune.
Un caro saluto ai miei piccoli lettori. Questa volta vorrei aiutarvi a capire un concetto molto importante nella fisica: quello di «calore». Ma come, potrebbe obbiettare qualcuno di voi, sappiamo perfettamente distinguere un oggetto caldo da uno freddo; è evidente che una pentola di acqua bollente possiede più calore di una lattina di aranciata appena tolta dal frigorifero! D’accordo, ma permettetemi una precisazione. Quello che siamo realmente in grado di affermare a proposito di corpi caldi o freddi, senza paura di essere smentiti, è che la temperatura di un oggetto che i nostri sensi avvertono come caldo è sicuramente superiore a quella di un oggetto che invece percepiamo come freddo. Ma, attenzione, questo non significa che il corpo più caldo debba necessariamente avere anche un maggiore contenuto calorico. Come vedremo meglio più avanti, un litro di acqua a 100 °C (gradi Celsius), per esempio, possiede la stessa quantità di calore di 10 litri di acqua a 10 °C. E come potete constatare le due temperature sono molto diverse! Ma, allora, che cos’è il calore e cos’è la temperatura?
Corpi caldi e corpi freddi: il calorico
I primi tentativi di spiegare cos’è il calore si basavano su un’osservazione che era davanti agli occhi di tutti: il calore si trasmette sempre dal corpo più caldo a quello più freddo. Un cucchiaino immerso in una tazza di caffè bollente si riscalda mentre il caffè nel frattempo si raffredda. Segno evidente che del calore è passato dal caffè più caldo al cucchiaino meno caldo, provocandone l’aumento di temperatura: avete mai visto accadere il contrario? Basandosi su questa evidenza, la cosa più logica, inizialmente, fu quella di considerare il calore come una sorta di fluido che passa da un corpo caldo a uno più freddo, un po’ come accade per l’acqua che scorre sempre da un livello più alto a uno più basso. A questo fluido fu dato il nome di «calorico»: quando un corpo perde calorico la sua temperatura si abbassa, quando invece lo acquista, la sua temperatura aumenta. Il ragionamento non faceva una grinza! Ovviamente, per come era stata costruita questa teoria, la quantità totale di calorico doveva rimanere sempre la stessa e conservarsi: tanto calorico perde il corpo che si raffredda, altrettanto calorico deve essere acquistato dal corpo che si riscalda.
Il merito di aver messo in discussione questo modo di vedere le cose viene generalmente attribuito all’americano Benjamin Thomson, più noto come conte Rumford di Baviera. Siamo verso la fine del XVIII secolo e Thomson era stato incaricato dal principe elettore di Baviera di far costruire dei cannoni per rinforzare la difesa dei confini, minacciati dal dilagare della Rivoluzione Francese. Osservando il processo di lavorazione di questi cannoni, Thomson si accorse che quando il corpo del cannone veniva alesato, cioè trapanato per realizzare il foro cilindrico della canna, sia il corpo del cannone sia la punta del trapano (ma anche i trucioli metallici prodotti dalla lavorazione) subivano un forte aumento di temperatura. Sembrava che del calore venisse creato in continuazione, anziché conservarsi come invece prevedeva la teoria del calorico. Thomson fece, allora, delle prove più sistematiche misurando l’aumento di temperatura che si verificava quando nell’operazione di foratura venivano utilizzati utensili meno affilati. In uno di questi esperimenti fu usata acqua per raffreddare la punta del trapano e, con grande stupore dei presenti, l’acqua si riscaldò a tal punto da essere portata all’ebollizione (fenomeno che in precedenza non era mai stato osservato in assenza di una fiamma!). Thomson concluse allora che il calore non poteva essere una sostanza materiale, il fantomatico calorico, per l’appunto, dal momento che non esisteva un limite alla sua produzione. Doveva per forza trattarsi di un effetto dell’attrito prodotto dallo sfregamento della punta del trapano contro la parete del foro.
Il problema, quindi, era stato correttamente individuato… ma non risolto. Che cos’era questo non ben precisato effetto dell’attrito, invocato dallo scienziato americano?
Calore e temperatura
Per rispondere alla domanda si dovette attendere fino alla metà del XIX secolo, quando gli scienziati riuscirono finalmente a comprendere come è fatta realmente la materia. Grazie a questi studi, ormai sappiamo che la materia è composta da un gran numero di particelle (gli atomi e le molecole) le quali – cosa molto importante – non stanno mai ferme ma sono in continua agitazione: oscillano avanti e indietro rispetto alla posizione occupata nel materiale, come tante palline appese a un molla. Queste oscillazioni, che ovviamente non siamo in grado di osservare direttamente perché avvengono su scale microscopiche, non sono affatto casuali, ma dipendono in maniera stringente dallo stato termico del materiale: quanto più alta è la sua temperatura, tanto più cresce l’agitazione di atomi e molecole. La temperatura di un corpo (il nostro compreso), quindi, non è altro che una misura dello stato di agitazione delle particelle che lo compongono. Se ci pensate bene, è una cosa davvero stupefacente. Noi non riusciamo a vedere gli atomi e le molecole di un oggetto perché son troppo piccoli per poter essere osservati (anche con un microscopio), ma riusciamo ad apprezzare i loro movimenti attraverso la temperatura del materiale!
Ma allora, se la temperatura non è altro che una misura dello stato di agitazione di atomi e molecole, che cosa rappresenta il calore di un corpo? Il calore – questa è la risposta corretta – è una forma di energia: l’energia «termica». Si tratta dell’energia posseduta dagli atomi e dalle molecole di un oggetto a causa del loro continuo movimento. Poiché, atomi e molecole hanno una (anche se piccola) massa e non stanno mai fermi, significa che possiedono quella forma di energia a cui i fisici danno il nome di energia «cinetica» che vuol dire energia «di movimento». Qualunque oggetto in movimento, infatti, possiede una certa dose di energia cinetica e lo si può facilmente verificare osservando le conseguenze di un suo eventuale impatto con un altro oggetto. Pensate per esempio cosa può provocare un sasso che (per sbaglio, s’intende!) avete lanciato nella direzione di una vetrata o un vaso di fiori che (accidentalmente, s’intende) cade da un balcone del terzo piano sulla vostra auto parcheggiata proprio li sotto… È chiaro che in entrambi i casi il danno provocato dall’impatto dipende dalla massa e dalla velocità del corpo in movimento, e quindi, in ultima analisi, da quant’è la sua energia cinetica. Quando un oggetto è fermo, e quindi non possiede questa forma di energia, non può far danno: i fisici si limitano a dire che «non compie lavoro».
Calore ed energia cinetica degli atomi o delle molecole
Come qualunque altra forma di energia, anche quella termica può essere acquistata oppure ceduta. La punta del trapano usato per forare i cannoni ai tempi di Thomson, per esempio, trasferiva per effetto dell’attrito, parte della sua energia (meccanica) ai trucioli metallici e alle pareti della canna che di conseguenza si riscaldavano, aumentando così l’agitazione delle sue molecole e di conseguenza anche la propria energia termica. Stabilito, pertanto, che il calore è l’energia posseduta dagli atomi o dalle molecole di un oggetto in virtù del loro continuo movimento, è evidente che il contenuto calorico (o, se preferite, l’energia termica) dell’intero oggetto non è altro che la somma dei tanti piccoli contributi forniti da ciascuno dei suoi numerosi atomi o molecole. Questo spiega perché un litro d’acqua a 100 °C (gradi Celsius) possiede lo stesso contenuto di calore di 10 litri di acqua a 10 °C. È vero che le molecole di acqua a 100 °C, prese singolarmente hanno un’energia 10 volte superiore a quella delle molecole di acqua a 10 °C, ma, in questo caso, sono anche 10 volte meno numerose. Di conseguenza la somma dei contributi calorici di tutte le molecole, nei due casi, è esattamente lo stesso.
Tuttavia, una differenza (non proprio trascurabile) esiste. Il calore posseduto da un corpo portato a 100 °C è più facilmente utilizzabile di quello di un qualunque altro corpo che si trovi a 10 °C. Provate a far cuocer gli spaghetti in una pentola riempita con acqua a 10 °C! Potete mettere nella pentola quanta acqua volete per aumentare il suo contenuto calorico, ma i vostri spaghetti rimarranno comunque irrimediabilmente crudi. Per questo motivo, la grande quantità di calore (e quindi di energia) immagazzinata nell’acqua dei mari che ricoprono il nostro pianeta – enormemente più grande dell’energia che tutte le centrali elettriche esistenti sarebbero in grado di produrre contemporaneamente – non può essere sfruttata a causa della temperatura troppo bassa.
Esperimento
Vi propongo ora un semplice esperimento che vi permetterà di verificare come il calore possa essere generato senza bisogno di alcuna sorgente termica (proprio come aveva osservato Thomson nella foratura dei cannoni).
Vi serve solo un pezzo di fil di ferro non troppo rigido, lungo circa 30 centimetri.

Primo passo
Segnate con un pennarello il punto centrale dello spezzone di filo, in modo da renderlo ben visibile.
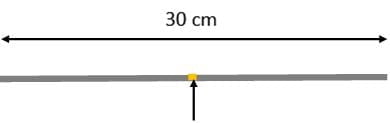
Secondo passo
Piegate ripetutamente (almeno dieci volte) prima in su poi in giù il pezzo di filo attorno al suo punto centrale.
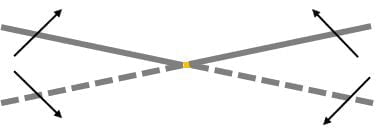
Se ora toccate questo punto vi accorgerete che la sua temperatura è aumentata rispetto a quella iniziale ed è anche più alta di quella delle parti più lontane del filo.
Spiegazione
Le molecole della porzione di filo sottoposta a ripetuti piegamenti modificano la propria posizione (all’interno del filo) andando così a interferire con quelle vicine. L’attrito generato da questo continuo «sfregamento» fa aumentare la temperatura del filo in quella regione. Il fenomeno è analogo a quello osservato da Thomson durante la foratura dei cannoni.
Sergio Musazzi
(Ricercatore e divulgatore scientifico)
