Albert Einstein considerava «sacra» quella curiosità infantile tipica dei bambini, ma anche dei grandi scienziati e che è spesso mortificata da approcci ludici o fantasiosi se non addirittura aridamente formalistici. L’autore, in questa rubrica, raccoglie la sfida di coniugare la semplicità e il rigore concettuale e linguistico.«Zio Albert» invita i suoi piccoli lettori ad affinare lo sguardo e accorgersi della particolare forma delle gocce come le gocce d’acqua a tutti familiari, per scoprire con lui la forza responsabile.
Un caro saluto ai miei piccoli lettori. Questa volta vorrei iniziare col chiedervi: avete mai osservato le goccioline di rugiada che a volte si formano sui fili delle ragnatele dopo una fresca notte primaverile? Se ci avete fatto caso, avrete sicuramente notato che hanno tutte una forma pressoché sferica. Una cosa molto simile si verifica anche quando piove subito dopo che la vostra auto (pardon, l’auto di vostro padre!) è stata lavata e sulla carrozzeria è stata passata la cera. Le gocce d’acqua che si depositano sulla carrozzeria hanno una forma sferica alquanto panciuta – insomma, assomigliano tutte a delle mezze sfere. Al contrario, quando vi cade una goccia di alcol sulla superficie del tavolo (non importa di che materiale sia fatto) assume sempre una forma molto schiacciata, ben lontana dal ricordare una semisfera.
Questi fenomeni sono tutti riconducibili a una particolare proprietà delle sostanze liquide nota come «tensione superficiale», una caratteristica questa che varia da liquido a liquido, ed è responsabile di alcuni dei loro comportamenti. Una verifica piuttosto semplice della sua esistenza può essere fatta, per esempio, osservando la superficie di uno stagno. Questa superficie, infatti, nonostante sia liquida, si comporta come una sottile membrana elastica, consentendo ad alcuni insetti acquatici di camminare tranquillamente sul pelo dell’acqua senza correre il pericolo di sprofondare. Curioso, no? Cerchiamo, allora, di capire, perché esiste la tensione superficiale e perché proprio da essa dipende la forma delle gocce.
Le forze di coesione
I liquidi, tutti i liquidi, sono composti da minuscole particelle (degli aggregati di atomi chiamati «molecole») che stanno insieme perché si attirano fra di loro. Detto in termini un po’ più rigorosi, sulle particelle di un liquido agiscono delle forze di natura attrattiva: le cosiddette «forze di coesione».
Queste forze sono molto importanti perché sono quelle che rendono un liquido diverso da un solido o da un gas e, soprattutto, sono quelle che ne determinano alcune fondamentali proprietà come, per esempio, il fatto che un liquido si adatta sempre alla forma del recipiente che lo contiene. Se le forze di coesione fossero più intense, infatti, il liquido non riuscirebbe a scorrere e a occupare il volume del recipiente in cui viene versato. In pratica si trasformerebbe in un solido.
Se, invece, fossero meno intense, non sarebbero in grado di tenere insieme le particelle del liquido che, di conseguenza, se ne andrebbero ciascuna per conto proprio, trasformandosi così in un gas che, proprio per questo motivo, diversamente dai liquidi, occupa sempre tutto lo spazio che ha a disposizione. Le forze di coesione sono anche responsabili dell’insorgere della tensione superficiale e, di conseguenza, anche della forma delle gocce. Vediamo in che modo.
La tensione superficiale
Come dicevamo, qualunque particella di un liquido viene attirata da tutte quelle che la circondano. Ma, attenzione, non tutte le particelle del liquido si trovano nella medesima situazione. Mentre quelle poste sotto la sua superficie sono completamente circondate da altre particelle, quelle che invece formano lo strato superficiale non lo sono. Queste ultime, infatti, hanno altre compagne sia di fianco sia sotto di loro, ma non ne hanno al di sopra. E questo fa la differenza! Una particella che si trovi sotto la superficie del liquido, infatti, viene attirata con la stessa intensità in tutte le direzioni (perché è completamente circondata da altre particelle) e di conseguenza non esiste una direzione privilegiata in cui viene spinta o tirata.
Questa particella, pertanto, non risente dell’azione di alcuna forza. Per capirci, è la stessa situazione di quando due vostri amici vi prendono per le braccia ed iniziano a tirarvi con la stessa forza da parti opposte. Il risultato netto è che voi rimanete fermo, come se nessuno vi stesse sollecitando, perché nonostante gli sforzi dei vostri amici le forze da loro esercitate si equilibrano. Naturalmente le cose cambierebbero se intervenisse un terzo amico che inizia a spingervi o tirarvi in un’altra direzione. Questo, seppure con modalità diverse, è quello che capita anche alle particelle che si trovano sulla superficie del liquido.
Queste ultime, infatti, sono attirate orizzontalmente da tutte quelle che si trovano al loro fianco ma verticalmente solo da quelle che si trovano sotto di loro, trovandosi così in una situazione di non equilibrio. Pertanto, mentre le forze di attrazione esercitate orizzontalmente dalle altre particelle superficiali si equilibrano reciprocamente (per ogni particelle che tira in una certa direzione ce n’è sempre un’altra che tira nella direzione opposta), le forze di attrazione (verticali) esercitate dalle particelle sottostanti non hanno chi le possa bilanciare (vedi figura).
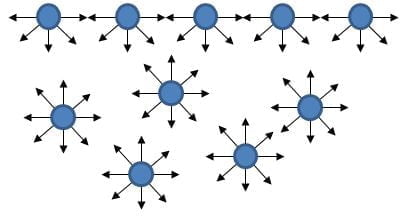
Il risultato netto è che su ciascuna delle particelle che formano lo strato superficiale di un liquido agisce una forza che la tira verso il basso. Questo fa sì che lo strato superficiale del liquido risulti leggermente compresso – aumenta cioè la coesione fra ogni sua particella e le vicine – creando in questo modo una sottile pellicola elastica (che è la responsabile dei fenomeni legati alla tensione superficiale). Detto in termini meno rigorosi, possiamo pensare che le particelle di liquido superficiali, avendo meno vicine da attirare, possano tirare con più forza quelle che hanno a disposizione (le loro confinanti), costruendo in questo modo uno strato di particelle che si tengono saldamente per mano.
Perché le gocce sono sferiche?
A questo punto siamo anche in grado di capire perché le gocce debbano essere sferiche. Il motivo è semplice. Poiché, come abbiamo visto, le particelle superficiali di un liquido formano una sottile membrana elastica, quelle sottostanti rimangono intrappolate all’interno della goccia e non riescono a emergere per raggiungere la sua superficie. Quest’ultima, perciò, non può crescere e quindi tende sempre a essere il meno estesa possibile. Orbene, la matematica ci insegna che, a parità di volume, la forma geometrica che possiede la minor superficie (e quindi che occupa meno spazio) è proprio quella sferica. E questo spiega perché le gocce debbano assumere proprio quella forma. Naturalmente, la tendenza di un liquido a formare gocce sferiche dipende dall’intensità delle forze di coesione (che varia da liquido a liquido).
Nel mercurio – l’unico metallo allo stato liquido a temperatura ambiente – per esempio, le forze di coesione sono così forti che piccole quantità di mercurio formano goccioline quasi sferiche anche quando vengono deposte su una superficie liscia. Cosa che avrete sicuramente notato anche voi se vi è malauguratamente capitato di rompere un termometro a mercurio facendolo cadere sul pavimento di casa vostra. Nei liquidi come l’alcol o l’acqua saponata, invece, le forze di coesione sono molto piccole, e quindi una loro goccia deposta su una superficie liscia tende ad appiattirsi e a slabbrarsi e a non assumere una forma sferica.
Per verificare l’esistenza della tensione superficiale vi propongo un semplice esperimento.
Esperimento
Vi servono solo un bicchiere, una graffetta metallica e del sapone liquido (quello per i piatti va benissimo).

Primo passo
Riempite il bicchiere di acqua fino all’orlo.
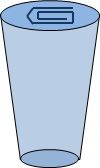
Secondo passo
Posate delicatamente la graffetta sulla superficie dell’acqua (il trucco consiste nell’appoggiarla sul bordo del bicchiere e spingerla verso il centro). Se non ci riuscite, potete porre la graffetta su un pezzo di carta velina e appoggiare quest’ultima sull’acqua. Spingete poi la carta velina sul fondo del bicchiere aiutandovi con uno stuzzicadenti. Noterete che, nonostante si tratti di un oggetto metallico, in contrasto con quanto previsto dalla legge di Archimede, la graffetta non affonda ma galleggia.
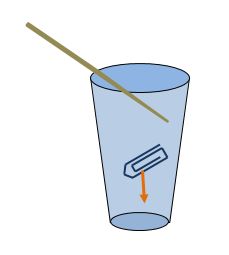
Terzo passo
Se ora inserite nell’acqua uno stuzzicadenti che avete precedentemente intinto in un detersivo liquido, la graffetta cesserà di galleggiare e sprofonderà quasi immediatamente sul fondo del bicchiere.
Spiegazione
La graffetta galleggia perché è sostenuta dalla sottile pellicola che si forma sulla superficie dell’acqua a causa della tensione superficiale. La graffetta cessa di galleggiare quando l’acqua contenuta nel bicchiere viene contaminata dal detersivo perché la presenza del sapone riduce le forze di coesione delle particelle liquide e di conseguenza anche la tensione superficiale dell’acqua.
P.S.
Poiché i detersivi riducono la tensione superficiale dell’acqua, il loro utilizzo consente all’acqua di penetrare facilmente nei piccoli spazi e quindi di rimuovere lo sporco anche nei punti più difficilmente raggiungibili.
Sergio Musazzi
(Ricercatore e divulgatore scientifico)
