Sarebbe bello se la Befana portasse diamanti al posto del carbone! Il diamante infatti è carbonio puro esattamente come la grafite che si usa per fare le matite. La cosa è stata dimostrata già nel 1772 da Antoine-Laurent de Lavoisier, che ha bruciato in ossigeno puro sia il diamante che la grafite mostrando che si forma la stessa quantità di anidride carbonica.
Il carbonio entra per lo 0,18 % in peso nella composizione della crosta terrestre; è quindi il decimo elemento più abbondante, dopo ossigeno, silicio, alluminio, ferro, calcio, magnesio, sodio, potassio e titanio. Costituisce il 23% del corpo umano, preceduto dall’ossigeno solo perché la quantità di acqua è circa il 60% del peso del corpo. Il carbonio è l’elemento chimico fondamentale in tutte le molecole che costituiscono gli esseri viventi.
Il carbonio puro si presenta in due forme cristalline: la grafite e il diamante. La grafite è la forma stabile, a temperatura e pressione ambiente, mentre il diamante è la forma stabile a pressioni superiori a 50.000 atmosfere (vedi il grafico qui sotto).
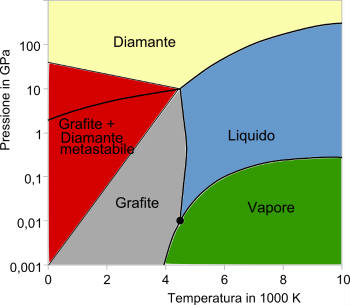
Solo l’estrema difficoltà a trasformarsi in grafite a temperatura ambiente (si dice che è metastabile) fa sì che nessuno abbia mai visto un diamante trasformarsi spontaneamente in grafite: tranquilli, i gioielli sono al sicuro!
La formazione dei diamanti può quindi avvenire solo ad altissime pressioni e queste si formano naturalmente solo a grandi profondità (intorno ai 200 km) e a temperature attorno ai 1000 °C in particolari condizioni geochimiche.
Il ciclo del carbonio ha visto aumentare il suo interesse per la nota discussione sull’effetto delle emissioni di anidride carbonica sul riscaldamento globale. I principali assorbitori di anidride carbonica sono notoriamente i vegetali e le masse oceaniche ma sono presenti meccanismi che portano al sequestro di carbonio superficiale negli strati profondi della terra. Per questo si è costituito nel 2009 l’Osservatorio del carbonio profondo per favorire lo studio del ciclo del carbonio oltre gli scambi superficiali.
Nell’ambito delle attività promosse dall’Osservatorio, nel primo numero di novembre della rivista Nature Communications è stato pubblicato un articolo in cui si dimostra, mediante un modello matematico della chimica in un mezzo acquoso a grande profondità, come negli strati profondi della litosfera, a circa 500.000 atmosfere e 900 °C, sia possibile la formazione di diamanti a partire dal carbonio contenuto nell’acqua sotto forma di carbonato o bicarbonato, per precipitazione dovuta a un brusca diminuzione del pH (quindi un aumento di acidità) e per l’interazione con le rocce.
La litosfera è la parte esterna rigida della Terra, comprende la crosta terrestre e si estende fino a circa 80 km sotto gli oceani e a 200 km sotto i continenti. Al di sotto si trova uno strato parzialmente fluido, molto viscoso, che costituisce la parte superiore del mantello ed è la causa del movimento delle placche che spiegano la dinamica della crosta terrestre, come per esempio la formazione delle montagne e l’origine dei terremoti.
La novità dello studio è data dal fatto che, finora, il meccanismo più accreditato di formazione dei diamanti non prevedeva la presenza di acqua e quindi non lo riteneva dipendente dal pH. D’altra parte il meccanismo spiega i dati sperimentali, anch’essi pubblicati su Nature nel 2015 (n. 524) , che rivelano le tracce di una soluzione salina (in particolare cloro e sodio) concentrata alla superficie di diamanti microscopici, cosa che fa supporre che si siano formati da acqua marina che è penetrata negli stati profondi della litosfera.
I diamanti che si formano in questo modo hanno dimensioni molto inferiori al millimetro, quindi non sono interessanti né in gioielleria né per le numerose applicazioni tecnologiche, tuttavia le condizioni meno restrittive in cui si formano fanno pensare che il meccanismo sia molto diffuso e quindi apre una finestra nuova sulla comprensione del ciclo del carbonio.
Questo non vuol dire che sicuramente gli scambi tra anidride carbonica atmosferica e superficie terrestre saranno rivoluzionati ma è un sicuro indice di quanto il meccanismo sia ancora poco conosciuto.
